- Частота встречаемости
- Виды гипогонадизма
- Причины и механизм развития
- Диагностика гипогонадизма как причины бесплодия
- Принципы лечения
- Прогноз по заболеванию
- Общие сведения
- Причины эндокринного бесплодия
- Симптомы эндокринного бесплодия
- Диагностика эндокринного бесплодия
- Лечение эндокринного бесплодия
- Прогноз при эндокринном бесплодии
- Профилактика эндокринного бесплодия
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
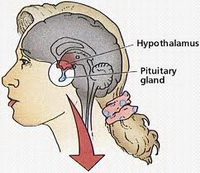
Гипогонадотропный гипогонадизм (ГГ) — заболевание, в основе которого лежит гипоталамо-гипофизарная недостаточность, сопровождающаяся задержкой полового развития центрального генеза, дефицитом эстрогенов.
Краткая информация о гипоталамусе, гипофизе и о механизмах работы данных органов изложена в статьях: «Бесплодный брак. Физиология женской репродуктивной системы» и «Бесплодный брак. Репродуктивная система женщины».
Частота встречаемости
Данный вид бесплодия встречается в 15-20% случаев аменореи.
Виды гипогонадизма
По времени развития различают врождённый и приобретённый ГГ.
По уровню повреждения различают гипоталамическую и гипофизарную формы.
По степени тяжести выделяют лёгкую, средней тяжести и тяжёлую формы.
Причины и механизм развития
 Врождённый необратимый гипогонадизм обусловлен генетическими причинами — мутации гена рецептора — гонадотропин релизинг гормона (Гн-РГ), мутации генов содержащих информацию о гормонах — ЛГ и ФСГ.
Врождённый необратимый гипогонадизм обусловлен генетическими причинами — мутации гена рецептора — гонадотропин релизинг гормона (Гн-РГ), мутации генов содержащих информацию о гормонах — ЛГ и ФСГ.
Приобретённая недостаточность гонадотропинов — следствие воздействия внешних неблагоприятных факторов и может быть обратимой:
• аменорея (отсутствие менструации) при неврогенной анорексии (отказе от еды)
• при быстром снижении массы тела
• аменорея физической нагрузки – при чрезмерных физических нагрузках. Данное явления характерно для спортсменок.
• психогенная аменорея. Исчезновение месячных вследствие психического перенапряжения или стрессов
• послеродовый гипопитуитаризм (синдром Шиена). Как правило появляется вследствие обильной кровопотери в родах.
По причине недостаточности гипоталамо-гипофизарной системы отсутствует её циклическое стимулирующее влияние на яичники, развивается вторичная недостаточность яичников, обусловливающая отсутствие овуляции и дефицит эстрогенов. При этом анатомически и функционально яичники полноценны. Также изначально анатомически и функционально полноценны все половые органы женщины, но в условиях длительного состояния сниженного уровня эстрогенов органы репродукции претерпевают определенные дегенеративные изменения, несовместимые с наступлением беременности.
Бесплодие при ГГ относится к эндокринным формам. Основная причина бесплодия у женщин с ГГ — отсутствие роста фолликулов и овуляции. Это происходит из-за отсутствия стимулирующего влияния гонадотропинов (ФСГ, ЛГ) на фолликулярный аппарат яичников. Отсутствие гонадотропинов может быть обусловлено нарушением выработки гипофизом данных гормонов в условиях адекватной секреции Гн-РГ или отсутствием гипоталамической секреции Гн-РГ. Так же встречаются формы характеризующиеся дефектами гормонов Гн-РГ, ЛГ, ФСГ или дефектами их рецепторов на поверхности клеток мишеней.
Диагностика гипогонадизма как причины бесплодия
 Отсутствие менструации — ведущий симптом гипогонадотропного гипогонадизма, как врождённого, так и приобретённого. Гипогонадотропная аменорея развивается на фоне врождённой или приобретённой недостаточности синтеза Гн-РГ гипоталамусом, гипофизарной недостаточности (дефицит ЛГ, ФСГ) или имеет смешанное гипоталамо-гипофизарное происхождение, может быть первичной или вторичной. Чаще встречается первичная аменорея (когда менструации и не начинались) -65%, у части женщин (35%) могут быть 2-5 спонтанных менструаций, после чего менструации исчезают — данное явление называют вторичной аменореей.
Отсутствие менструации — ведущий симптом гипогонадотропного гипогонадизма, как врождённого, так и приобретённого. Гипогонадотропная аменорея развивается на фоне врождённой или приобретённой недостаточности синтеза Гн-РГ гипоталамусом, гипофизарной недостаточности (дефицит ЛГ, ФСГ) или имеет смешанное гипоталамо-гипофизарное происхождение, может быть первичной или вторичной. Чаще встречается первичная аменорея (когда менструации и не начинались) -65%, у части женщин (35%) могут быть 2-5 спонтанных менструаций, после чего менструации исчезают — данное явление называют вторичной аменореей.
Дефицит эстрогенов в организме женщины обусловливает характерные особенности внешности:
• Тип телосложения евнухоидный: высокий рост за счёт увеличения длины ног, увеличение длины рук, уменьшение поперечных размеров таза, увеличение ширины плеч.
• Вторичные половые признаки недоразвиты, реже отсутствуют, особенно это касается молочных желёз.
• Молочные железы у женщин с ГГ недоразвиты, иногда значительно, но могут быть нормально развиты, в зависимости от выраженности дефицита эстрогенов. При рентгенологическом или УЗИ исследовании часто выявляют полное замещение железистой ткани молочной железы жировой тканью с участками уплотненной соединительной ткани преимущественно в преареолярных (околососковых) областях. У части больных (18%) обнаруживают фиброзно-кистозную мастопатию.
• Оволосение в подмышечных впадинах и на лобке скудное или умеренное.
• Гинекологическое исследование выявляет гипоплазию наружных и внутренних половых органов. Слизистая оболочка влагалища тонкая, сухая, неэластичная. Шейка матки уменьшена, наружный зев точечный. Матка значительно уменьшенных размеров, иногда не удаётся прощупать матку отдельно от шейки. Яичники так же не прощупываются. Гипоплазия (недоразвитие) матки более выражена, чем недоразвитие яичников. Выраженное уменьшение размеров матки и яичников выявляют и при УЗИ органов малого таза.
Лабораторно инструментальные исследования
Основа диагностики ГГ, как и других форм эндокринного бесплодия, это гормональное исследование.
Характерные показатели при гипогонадизме:
 Низкие концентрации гонадотропинов и эстрадиола в сыворотке крови (ЛГ 2,5-4,1 МЕ/л; ФСГ 1,5-2,9 МЕ/л; эстрадиол: 50-100 пмоль/л) при нормальных значениях других пептидных и стероидных гормонов.
Низкие концентрации гонадотропинов и эстрадиола в сыворотке крови (ЛГ 2,5-4,1 МЕ/л; ФСГ 1,5-2,9 МЕ/л; эстрадиол: 50-100 пмоль/л) при нормальных значениях других пептидных и стероидных гормонов.
1. Ввиду низкой эстрогенной насыщенности прогестероновая проба и проба с кломифеном у пациенток с ГГ отрицательная.
2. Циклическая гормональная проба — положительная.
Приведенные выше примеры лабораторной диагностики носят своей целью определение функционального состояния репродуктивной системы.
• ГГ с лёгкой степенью гипоталамо-гипофизарной недостаточности. При позднем наступлении менструации с нерегулярными скудными выделениями менструации исчезают вовсе. Телосложение пропорциональное. Молочные железы развиты с жировым замещением железистой ткани. Размеры матки и яичников соответствуют возрасту 12-13 лет. Уровни гонадотропинов в крови: ЛГ 5,8 МЕ/л (3,6-9,3 МЕ/л), ФСГ 2,6 МЕ/л (1,3-3,8 МЕ/л), эстрадиол — 50 пмоль/л (25,7-75,3 пмоль/л).
1. УЗИ органов малого таза для определения степени гипоплазии матки и яичников
2. липидограмма
3. исследование минеральной плотности костной ткани для выявления и профилактики возможных системных нарушений на фоне длительной гипоэстрогении
• ГГ с умеренной степенью гипоталамо-гипофизарной недостаточности. При наступлении менструации, но после 2-4 редких менструаций цикл исчезает. Телосложение диспропорциональное. Молочные железы недоразвиты, уменьшены в размере с жировым замещением железистой ткани. Размеры матки и яичников соответствуют возрасту 10-11 лет. Уровни гонадотропинов в крови: ЛГ 2,0 МЕ/л (1,7-2,5 МЕ/л), ФСГ 1,3 МЕ/л (1,1-1,6 МЕ/л), эстрадиол 30 пмоль/л (22,8-37,2 пмоль/л).
• ГГ с тяжёлой степенью гипоталамо-гипофизарной недостаточности. Полное отсутствие менструации, клинически больные характеризуются евнухоидными чертами телосложения. Молочные железы визуально отсутствуют или очень слабо развиты, с полным жировым замещением железистой ткани. Размеры матки и яичников женщины соответствуют таковым в возрасте 2-7 лет. Уровни гонадотропинов в крови: ЛГ 1,8 МЕ/л (1,3-2,4 МЕ/л), ФСГ ниже 1 МЕ/л, эстрадиол: ниже 30 пмоль/л.
Принципы лечения
 При гонадотропной недостаточности гипофиза единственным методом достижения роста фолликула в яичниках, овуляции, а следовательно, и беременности является применение заместительной терапии препаратами — гoнадотропинами. При повреждении гипоталамуса альтернативным способом лечения бесплодия может быть назначение гонадолиберинов, стимулирующих гонадотропную функцию гипофиза.
При гонадотропной недостаточности гипофиза единственным методом достижения роста фолликула в яичниках, овуляции, а следовательно, и беременности является применение заместительной терапии препаратами — гoнадотропинами. При повреждении гипоталамуса альтернативным способом лечения бесплодия может быть назначение гонадолиберинов, стимулирующих гонадотропную функцию гипофиза.
Лечение бесплодия складывается из двух этапов: подготовительный этап и индукция овуляции.
1. На подготовительном этапе производят заместительную циклическую гормонотерапию последовательным назначением эстрогенов и гестагенов с целью коррекции гормонального статуса женщины. Так же производится стимулирование роста и развития женских половых органов: увеличения размеров матки, роста эндометрия, формирования рецепторного аппарата в органах-мишенях, что повышает эффективность последующей стимуляции овуляции. Длительность подготовительной терапии определяется в зависимости от выраженности гипогонадизма и составляет в среднем 3-12 месяцев.
2. Индукция овуляции производится гонадотропинами и преследует цель – осуществление овуляции. Адекватность назначенного лечения оценивается посредством УЗИ исследования фолликулов яичников. Адекватность дозы применяемых препаратов оценивают по динамике роста фоллликулов (в норме — 2 мм в сутки). При медленном росте фолликулов дозу увеличивают, при слишком быстром росте — снижают. Медикаментозное лечение продолжают до образования зрелых фолликулов диаметром 18-20 мм. Затем в/м однократно вводят определенную дозу хорионического гонадотропина (ХГЧ). Под контролем УЗИ наблюдают за овуляцией – отсутствие доминантного фолликула говорит о том, что произошла овуляция.
После констатации овуляции проводят поддержку лютеиновой фазы цикла препаратами из группы гестагенов.
Профилактика развития бесплодия при дефиците эстрогенов включает заместительную терапию. Исходя из механизме развития заболевания, общепризнанна необходимость проведения заместительной терапии женскими половыми гормонами — эстрогенами и гестагенами, цель которой — формирование женской внешности.
• В период полового созревания — для формирования женского типа телосложения, нормального развития половых органов, молочных желёз и вторичных половых признаков, а также для достижения нормальной массы костной ткани. Необходимы ранняя диагностика ГГ и своевременное назначение заместительной гормональной терапии (с 16-18 лет), продолжение её по возможности непрерывно до 20-23 лет.
• В репродуктивный период — перед индукцией овуляции в качестве подготовки к беременности желательна заместительная гормональная терапия в течение 3 месяцев. После беременности, родов и лактации необходима заместительная гормональная терапия виде длительных курсов минимум в течение 12 месяцев с целью профилактики остеопороза.
• В период после рождения ребенка — необходимы диагностика системных изменений, вызванных гормональными нарушениями и их коррекция с помощью заместительной гормональной терапии, фитотерапии и специфических препаратов для лечения остеопороза. Заместительную гормональную терапию при гипогонадотропном гипогонадизме у женщин можно продолжать до возраста естественной менопаузы (45-50 лет).
Прогноз по заболеванию
Автор: Ткач И.С. врач, хирург офтальмолог

Эндокринное бесплодие – комплекс гормональных нарушений, ведущих к нерегулярности овуляции или ее отсутствию у женщин и нарушению качества спермы у мужчин. В его основе могут лежать нарушения функций щитовидной железы, половых желез, гипоталамо-гипофизарной регуляции. Лечение эндокринного бесплодия заключается в устранении его причины, коррекции существующих нарушений и поддержании нормального гормонального фона. Нормализация нарушенных функций приводит к наступлению беременности в 70-80% случаев эндокринного бесплодия. В остальных случаях в настоящее время перспективным считается устранение эндокринного бесплодия методом ЭКО.

Общие сведения
Эндокринное бесплодие – комплекс гормональных нарушений, ведущих к нерегулярности овуляции или ее отсутствию у женщин и нарушению качества спермы у мужчин. В его основе могут лежать нарушения функций щитовидной железы, половых желез, гипоталамо-гипофизарной регуляции. Нормализация нарушенных функций приводит к наступлению беременности в 70-80% случаев эндокринного бесплодия. В остальных случаях в настоящее время перспективным считается устранение эндокринного бесплодия методом ЭКО. У каждой третьей бесплодной женщины причина бесплодия кроется в патологии эндокринной системы.
Понятие «эндокринного бесплодия» является собирательным, включающим различные нарушения механизмов гормональной регуляции менструального цикла: на гипоталамо-гипофизарно-яичниковом уровне, в системах ТТГ-щитовидная железа, АКТГ — кора надпочечников и др. Независимо от причин эндокринного бесплодия, в основе его развития лежит нарушение функции яичников, проявляющееся стойкой ановуляцией (отсутствием овуляции) или ее нерегулярностью.

Причины эндокринного бесплодия
Ановуляция может возникать при заинтересованности центральной нервной и иммунной систем, желез внутренней секреции, репродуктивных органов-"мишеней". Ановуляция, ведущая к эндокринной форме бесплодия, может развиваться в результате:
Обычно наблюдается после черепно-мозговых травм и травм грудной клетки, при опухолях гипоталамо-гипофизарной области и сопровождается гиперпролактинемией. Увеличение секреции пролактина ведет к торможению циклической продукции ЛГ и ФСГ гипофизом, угнетению функций яичников, редким менструациям (по типу олиго- и опсоменореи), развитию стойкой ановуляции и эндокринного бесплодия.
- Гиперандрогении яичникового или надпочечникового генеза
Присутствие в организме женщины небольшого количества андрогенов – мужских половых гормонов необходимо для полового созревания и правильного функционирования яичников. Усиленная секреция андрогенов может осуществляться яичниками либо надпочечниками, а иногда обеими железами одновременно. Чаще всего гиперандрогения у женщин сопровождает синдром поликистозных яичников, вызывая эндокринное бесплодие, ожирение, гирсутизм, кровотечения, олиго- и аменорею, двустороннее поражение яичников с изменением их морфологической структуры.
Надпочечниковая гиперандрогения чаще развивается в результате гиперплазии коры надпочечников с вторичным вовлечением яичников (вторичный поликистоз яичников).
- Нарушений функции щитовидной железы
Течение гипотиреоза и диффузного токсического зоба нередко сопровождается ановуляцией, вторичной гиперпролактинемий, эндокринным бесплодием, невынашиванием беременности, аномалиями плода.
- Дефицита эстрогенов и прогестерона (при недостаточности лютеиновой фазы)
Недостаток женских половых гормонов вызывает неполноценную секреторную трансформацию эндометрия, изменение функции маточных труб, препятствует прикреплению плодного яйца в полости матки. Это приводит к невынашиванию беременности или эндокринному бесплодию.
- Тяжелых соматических патологий (цирроза, гепатитов с выраженным повреждением клеток печени, туберкулеза, аутоиммунных и системных заболеваний соединительной ткани, злокачественных новообразований различной локализации и т. д.).
- Ожирения или недостатка жировой ткани
Жировая ткань в организме также выполняет эндокринную функцию, оказывая влияние на метаболические процессы в тканях, в т. ч. репродуктивной системы. Избыток жировых отложений вызывает гормональный дисбаланс, нарушение менструальной функции и развитие эндокринного бесплодия. В то же время, ограничение потребления жиров или резкая потеря массы тела нарушают нормальное функционирование яичников.
В основе синдрома лежит нарушение гипофизарно-яичниковой связи — нечувствительность рецепторного аппарата яичников к гонадотропинам, стимулирующим овуляцию, что проявляется аменореей, эндокринным бесплодием при нормально развитых половых признаках и высоком уровне гонадотропных гормонов. Повреждение яичников могут вызывать инфицирование вирусами краснухи, гриппа, патология ранее развивавшейся беременности, авитаминоз, голодание, стрессовые ситуации.
- Преждевременной менопаузы (синдрома истощенных яичников)
Вторичная аменорея, возникающая у молодых женщин до 35 — 38 лет, вызывает характерные для климактерического синдрома изменения и ведет к эндокринному бесплодию.
- Заболевания, связанные с мутациями половых хромосом
При заболеваниях, вызванных хромосомными аномалиями, наблюдается недостаточность женских половых гормонов, половой инфантилизм, первичная аменорея и эндокринное бесплодие (синдромы Марфана, Тернера).
Симптомы эндокринного бесплодия
Основными проявлениями эндокринного бесплодие являются невозможность наступления беременности и отклонения в менструальном цикле. Менструации могут наступать с задержками различной выраженности (от недели до полугода), сопровождаться болезненностью и обильными выделениями либо отсутствовать совсем (аменорея). Нередко отмечаются мажущие кровянистые выделения в межменструальный период.
У 30% пациенток с эндокринной формой бесплодия менструальные циклы носят ановуляторный характер и по своей продолжительности соответствуют нормальному менструальному циклу (21-36 дней). В таких случаях речь идет не о менструации, а о менструальноподобном кровотечении.
У пациенток отмечаются боль в нижних отделах живота или пояснице, выделения из половых путей, диспареуния, циститы. Могут наблюдаться напряжение и тяжесть в молочных железах, галакторея (выделения молозива из сосков), связанные с повышением уровня пролактина. Характерен синдром предменструального напряжения – ухудшение состояния накануне менструации. При гиперандрогении, сопровождающей эндокринное бесплодие, развиваются акне, гирсутизм или гипертрихоз, алопеция. Наблюдаются колебания артериального давления, развитие ожирение или похудание, образование стрий на коже.
Диагностика эндокринного бесплодия
При сборе анамнеза у пациенток с эндокринным бесплодием уточняется время начала менструаций, их обильность, болезненность, наличие в анамнезе (в т. ч. матери пациентки) нарушений менструальной функции, наличие и длительность отсутствия беременностей, при наличии – исход и осложнения беременностей. Необходимо выяснить, проводились ли ранее гинекологические операции и манипуляции, тип и длительность использования контрацепции.
Общий осмотр включает оценку роста пациентки (менее 150 см или более 180 см), наличие ожирения, вирилизма, развития молочных желез и вторичных половых признаков. Проводится консультация гинеколога, в ходе которой при гинекологическом осмотре выясняют форму и длину влагалища и матки, состояние шейки матки, параметрия и придатков. По данным общего и гинекологического осмотров выясняются такие причины эндокринного бесплодия, как половой инфантилизм, поликистоз яичников и др. Оценку гормональной функции яичников и наличие овуляции при эндокринном бесплодии определяют с помощью функциональных тестов: построения и анализа базальной температурной кривой, мочевого теста на овуляцию, ультразвукового мониторинга созревания фолликула и контроля овуляции.
По графику базальной температуры определяется наличие или отсутствие свершения овуляции. Базальная температурная кривая отражает уровень постовуляторной выработки яичниками прогестерона, подготавливающего эндометрий матки к имплантации оплодотворенной яйцеклетки. Базальная кривая строится на основе показателей утренней температуры, измеряемой ежедневно в одно и то же время в прямой кишке. При овуляторном цикле график температуры двухфазный: в день овуляции ректальная температура падает на 0,2-0,3 °С, а во второй фазе цикла, продолжающейся от 12 до 14 дней, поднимается в сравнении с температурой первой фазы на 0,5-0,6 °С. Ановуляторный менструальный цикл характеризуется монофазной температурной кривой (стойко ниже 37 °С), а недостаточность лютеиновой фазы проявляется укорочением второй фазы цикла менее 11-12 дней.
Подтвердить или опровергнуть факт совершения овуляции можно с помощью определения уровня прогестерона в крови и прегнандиола в моче. При ановуляторном цикле эти показатели во второй фазе крайне низки, а при недостаточной лютеиновой фазе — снижены в сравнении с овуляторным менструальным циклом. Проведение теста на овуляцию позволяет определить увеличение концентрации ЛГ в моче за 24 часа до совершения овуляции. Ультразвуковой мониторинг фолликулогенеза дает возможность проследить созревание в яичнике доминантного фолликула и высвобождение из него яйцеклетки.
Отражением функционирования яичников служит состояние эндометрия матки. В соскобе или биоптате эндометрия, взятого за 2-3 дня до ожидаемой менструации, при ановуляции и эндокринном бесплодии обнаруживается гиперплазия разной степени выраженности (железисто-кистозная, железистая, полипоз, аденоматоз) или секреторная недостаточность.
Для выяснения причин эндокринного бесплодия определяют уровни ФСГ, эстрадиола, ЛГ, пролактина, ТТГ, тестостерона, Т3, Т4, ДЭА-С (дегидроэпиандростерон-сульфата) на 5-7-й день в течение нескольких менструальных циклов. Проведение гормональных проб позволяет уточнить состояние различных звеньев репродуктивной системы при эндокринном бесплодии. Механизм проведения данных проб заключается в измерении уровня собственных гормонов пациентки после приема определенных стимулирующих гормональных препаратов.
При необходимости уточнения причин эндокринного бесплодия проводится рентген черепа, УЗИ щитовидной железы, яичников, надпочечников, диагностическая лапароскопия. Диагноз эндокринного бесплодия женщине устанавливается только после исключения мужского фактора бесплодия (наличие нормальной спермограммы), а также патологии со стороны матки, иммунологической и трубной форм бесплодия.
Лечение эндокринного бесплодия
Первый этап лечения эндокринного бесплодия включает нормализацию нарушенных функций эндокринных желез (коррекцию сахарного диабета, ожирения, деятельности надпочечников, щитовидной железы, удаление опухолей и т. д.). В дальнейшем проводится гормональная стимуляция созревания доминантного фолликула и овуляции. Для стимуляции овуляции назначается препарат кломифен цитрат, вызывающий увеличение секреции гипофизом фолликулостимулирующего гормона. Из наступивших после стимуляции кломифен цитратом беременностей 10% — многоплодные (чаще двойни и тройни).
В случае отсутствия беременности в течение 6 овуляторных циклов при стимуляции кломифен цитратом прибегают к лечению гонадотропинами: ЧМГ (человеческим менопаузальным гонадотропином), р-ФСГ (рекомбинантным фолликулостимулирующим гормоном), и ХГЧ (хорионическим гонадотропином человека). Лечение гонадотропинами повышает частоту наступления многоплодной беременности и развития побочных эффектов.
В большинстве случаев эндокринное бесплодие поддается гормональной коррекции, в остальных показано оперативное вмешательство. При синдроме поликистозных яичников прибегают к их клиновидной резекции лапароскопическим методом или лапароскопической термокаутеризации. После проведения лапароскопической термокаутеризации наблюдается наивысший процент наступления беременностей – от 80 до 90% случаев, т. к. исключается образование спаек в малом тазу.
При эндокринном бесплодии, отягощенном трубно-перитонеальным фактором или снижением фертильности спермы, показано проведение метода экстракорпорального оплодотворения (ЭКО) с пересадкой готовых к развитию эмбрионов в полость матки. Добиться наступления и вынашивания беременности у женщин с эндокринным бесплодием возможно только при комплексном решении данной проблемы.
Прогноз при эндокринном бесплодии
Сегодня эндокринное бесплодие не является приговором. Современная гинекология и эндокринология совместными усилиями успешно лечат 80% пациенток, применяя только медикаментозные методы. Если произошло восстановление овуляции и нет других факторов бесплодия, более 50% женщин беременеет на протяжении первых шести циклов стимулирующей гормональной терапии. Менее благоприятные результаты от медикаментозной терапии при эндокринном бесплодии, вызванном дисфункцией гипоталамо-гипофизарной регуляции.
Сразу после наступления беременности устанавливается тщательный контроль за ее развитием, госпитализация пациентки проводится при признаках самопроизвольного прерывания беременности. Нередко отмечаются дискоординация и слабость родовой деятельности.
Профилактика эндокринного бесплодия
Заботиться о профилактике эндокринных форм бесплодия необходимо с детского возраста. Уменьшение и предупреждение детских инфекций, хронического тонзиллита, ревматизма, гриппа, токсоплазмоза в детском и подростковом возрасте позволит избежать нарушений функции яичников и процессов гипоталамо-гипофизарной регуляции.
Превентивное значение имеет правильное эмоциональное и физическое воспитание девочек, т. к. функция яичников нередко страдает вследствие умственного перенапряжения, психологических и сексуальных травм. Неоспорим тот факт, что часто эндокринное бесплодие развивается после патологических родов, прерывания беременности, интоксикаций, воспалительных инфекций женской репродуктивной сферы, поэтому следует уделять внимание профилактике данных состояний.
Правильное ведение беременности, разумное использование некоторых лекарственных средств, в особенности гормонов во время беременности, помогут избежать врожденной гипофункции яичников и гиперплазии коры надпочечников у девочек.
В последние годы увеличивается число женщин, страдающих различными нарушениями менструальной функции, а также возрастает количество бесплодных браков, причем среди причин бесплодия доминирующую роль играют эндокринные факторы.
Гипоталамические и гипофизарные формы бесплодия у женщин; этиология и патогенез, клинико-лабораторные данные
В последние годы увеличивается число женщин, страдающих различными нарушениями менструальной функции, а также возрастает количество бесплодных браков, причем среди причин бесплодия доминирующую роль играют эндокринные факторы.
Этиология:
1. Патология гипофиза.
• Синдром Шихена (о. гипопитуитаризм).
• Гипофизарный гипогонадизм.
• Гиперпролактинемия (пролактинома, гипотиреоз, нейролептики ).
• Гипофизарный нанизм.
• Болезнь Иценко-Кушинга.
2. Патология гипоталамуса.
• Синдром Каллмена.
• Нейрогенная анорексия.
• Перетренированность, тяжелый физический и умственный труд.
• Синдром Бабинского-Фрелиха.
Патогенез:
Данные виды бесплодия являются гипогонадотропными формами гипогонадизма. Таким образом, имеются нарушения выработки гонадотропинов (ФСГ и ЛГ), что приводит в свою очередь к нарушению деятельность регулируемых ими яичников, а также снижению в крови содержания эстрогенов, прогестерона и в моче 17-КС. Таков механизм возникновения бесплодия при синдроме Шихена, гипофизарном нанизме и гипогонадизме, синдроме Каллмена, Бабинского-Фрелиха.
При болезни Иценко-Кушинга наблюдается недостаточная стимуляция яичников гонадотропинами за счет блокады зон аденогипофиза при гиперпродукции кортикотропина.
Особое внимание следует уделить патогенезу бесплодия при гиперпролактинемии. Увеличение выработки пролактина наблюдается при пролактиноме, гипотиреозе, а также применении нейролептиков. Различают следующие группы факторов, ведущих к гиперпролактинемии:
• операции на молочной железе и грудной клетке.
• стрессы.
• избыточная пальпация молочной железы.
• избыточное употребление пива.
• избыток жирной пищи.
Увеличенное количество пролактина вызывает блок выработки ФСГ и ЛГ, приводит к снижению количества эстрогенов, аменорее и атрофии половых органов, а также снижению выработки прогестерона. Увеличенное количество пролактина в крови, высокий уровень ТТГ и бесплодие могут свидетельствовать о развитии гипотиреоза.
Клинико-лабораторные проявления:
Диагностический поиск начинается с анализа жалоб и сбора анамнеза. Наиболее характерны жалобы на нарушение менструальной функции по типу олиго- или аменореи ( первичной или вторичной ), бесплодие ( первичное или вторичное ), иногда на выделения из сосков (галакторея). Особую группу составляют больные с жалобами на избыточный рост волос на лице и теле по мужскому типу ( гирсутизм ), вульгарные угри, жирную себорею, выпадение волос на голове (алопецию ) и др. Данный симптомокомплекс является отражением гиперандрогении и будет рассмотрен отдельно.
Клиническое обследование должно включать:
— оценку роста и массы тела с вычислением индекса массы тела;
— оценку фенотипа ( женский, мужской );
— оценку состояния кожи ( цвет, влажность или сухость, наличие стрий, себореи, вульгарных угрей, характер полового оволосения, состояние волос на волосистой части головы);
— оценка степени развития молочных желез, наличие или отсутствие галактореи, тяжистых или узловатых уплотнений;
— гинекологическое бимануальное исследование и осмотр шейки матки в зеркалах;
— оценку общего состояния ( заторможенность, отечность, артериальное давление, пульс, изменение черт лица, увеличение размера обуви и т.д. );
— регистрацию осмотических генетических стигм ( высокое небо, короткая шея, бочкообразная грудь и др.).
Кроме общеклинического исследования, применяются функциональные тесты — измерение базальной, или ректальной температуры в течение не менее 3-х месяцев, оценка состояния цервикальной слизи ( симптом «зрачка», симптом натяжения слизи, симптом арборизации), кольпоцитология вагинального мазка с подсчетом индекса созревания и кариопикнотического индекса.
При бесплодном браке обязательным является обследование мужа: (сперматограмма, посткоитальный тест, консультация андролога).
Для уточнения уровня нарушения репродуктивной и других систем используют весь спектр современных методов обследования, включающий ЭЭГ,РЭГ, рентгенологические методы, КТ,МРТ, УЗИ, лапароскопию, гистероскопию с морфологическим исследованием. Кроме того, в ряде случаев необходимо определение уровня гипофизарных ( ЛГ, ФСГ, ПРЛ, ТТГ, СТГ и АКТГ ) и стероидных гормонов — Э-2 и других фракций эстрогенов, прогестерона, тестостерона, андростендиона, дегидроэпиандростерона ( ДЭА ) и его сульфата, 17-гидроксипрогестерона, кортизола и т.п. При необходимости проводят генетическое обследование.
При одновременном снижении уровней Э-2, ЛГ и ФСГ на фоне нормального содержания пролактина речь идет о вторичной гипофункции яичников, обусловленной выпадением их стимуляции со стороны гипоталамо -гипофизарной системы, т.е. о гипогонадотропной гипофункции яичников.
К гипогонадотропной гипофункции яичников условно относят так называемую нормогонадотропную гипофункцию, при которой базальный уровень гонадотропных гормонов не снижен. Однако, при определении частоты и амплитуды секреторных импульсов ЛГ и ФСГ обнаруживают нарушение циклического ритма их секреции.
